最近,内分泌-糖尿病领域的权威刊物Diabetes延续在线发表了北京大学基础医学院杨吉春教授团队的两篇研究论文。论文揭示了以FAM3基因家族成员FAM3A及FAM3C为核心的非胰岛素依靠糖脂代谢调控网络。
课题组在前期研究中已揭示FAM3A是一个新线粒体蛋白,其在肝脏表达受克制的2型糖尿病及非酒精性脂肪肝发生过程中起紧张作用。然而,糖尿病发生时,肝脏FAM3A表达受克制的机制尚不清楚(Hepatology 2014)。课题组结合生物信息学展望和一系列细胞生物学手段,证明FAM3A是miR-423-5p的靶基因。miR-423-5p可直接克制FAM3A-ATP-CaM通路。在脂肪肝患者及糖尿病小鼠肝脏中,miR-423-5p表达非常升高。在糖尿病小鼠肝脏中克制miR-423-5p可改善高血糖及脂肪肝,而在正常小鼠肝脏中过表达miR-423-5p则导致肝脏糖脂代谢非常。在脂肪肝患者及糖尿病小鼠肝脏中,NFE2表达水平显明增长。肥胖发生时,肝脏NFE2表达被激活,其通过诱导miR-423-5p表达克制FAM3A-ATP-Akt通路,导致肝脏及全身糖脂代谢混乱。克制NFE2/miR-423-5p旌旗灯号轴激活FAM3A表达有可能成为2型糖尿病的新干预策略(Diabetes 2017 Apr 14. doi: 10.2337/db16-1172.[Epub ahead of print],http://diabetes.diabetesjournals.org/content/early/2017/04/13/db16-1172.long,博士生杨卫利是论文第一作者,杨吉春为论文通信作者)。目前,课题组已筛选到数种激活FAM3A表达的小分子,其表现了优秀的抗糖尿病、脂肪肝及肥胖结果(待投稿)。
在糖尿病小鼠肝脏组织中,FAM3基因家族另一成员FAM3C表达也明显降低。在糖尿病小鼠肝脏特异性过表达FAM3C基因后,小鼠高血糖、全身胰岛素抵抗及脂肪肝症状明显缓解。在糖尿病小鼠肝脏过表达FAM3C克制糖脂异生关键基因的表达。FAM3C通过诱导CaM表达进而激活Akt,且这一过程不依靠胰岛素及细胞外Ca2+内流。研究进一步揭示FAM3C通过激活HSF1调控CALM1表达,克制HSF1,能反转FAM3C对CALM1表达、Akt激活及糖异生克制的作用。在激活Akt通路的同时,FAM3C还克制mTOR-SREBP1C-FAS通路,克制肝脏脂质合成,缓解脂肪肝。本研究揭示了在肥胖状态下,肝脏FAM3C表达降落将会克制HSF1-CaM通路,导致糖代谢和脂代谢失调,而恢复FAM3C-HSF1-CaM旌旗灯号通路有利于改善肝脏糖脂代谢非常。(Diabetes 2017 Feb 28. doi: 10.2337/db16-0993.[Epub ahead of print],http://diabetes.diabetesjournals.org/content/early/2017/02/27/db16-0993.long,博士生陈真真和硕士生丁立伟是论文共同第一作者,杨吉春为论文通信作者)。目前,课题组已筛选到了几种能激活FAM3C表达的小分子,正在评估其抗糖尿病结果。
随着糖尿病病情的发展,胰岛素抵抗及胰岛功能衰竭进行性加重,现有的许多干预药物每每难以有用控制血糖。该系列研究揭示FAM3A及FAM3C分别从功能性激活及转录水平激活CaM-Akt通路,以非胰岛素依靠途径克制肝脏糖异生过程,缓解高血糖,为伴随紧张胰岛素抵抗的2型糖尿病及脂肪肝患者治疗提供了数个潜在的干预靶点。

FAM3A与FAM3C通过功能性及转录激活CaM,克制肝脏糖脂异生缓解糖尿病及脂肪肝
本课题受国家基金委良好青年基金及面上项目、科技部慢性病项目及北京市重点项目资助。杨吉春团队己在Hepatology、Diabetes、ATVB、J.B.C、JMCC、BBA及Nutr Rev等国际闻名期刊上发表SCI论文50余篇,总影响因子约360,其中第一及通信作者论文32篇;近年来以通信作者身份在Hepatology、Diabetes、NAR等国际闻名期刊上发表研究论文21篇,总影响因子约120。
编辑:山石
下一篇::工学院邹如强课题组在稳固高效电解水制氢催化剂材料研究中取得紧张进展
- 2017年天津大学成人高等教育招生简章
- 北京化工大学2018年成人高考招生简章
- 2018年首都体育学院成人高等教育招生简章
- 北京农学院2018年成人高等教育招生简章
- 2018年北京服装学院成人高考招生简章
- 北京第二外国语学院继续教育学院成考招生简章
我有话说
最新文章
- 1教育部专家组来我院开展基本

根据教育部工作部署,2018年5月24日教育部直......
- 2北京市委常委、宣传部部长杜

7月16日下午,中共北京市委常委、宣传部部长......
- 3焦宁教授研究团队在醇类分子

2018年7月6日,NatureCommunications(《自然......
- 4Nature Biotechnology报道生

2018年7月9日,北京大学生命科学学院、北大-......
- 5物理学院吕劲团队发现新型二

近年来,半导体行业总是笼罩在摩尔定律难以为......
热门文章
- 1电镜实验室高鹏等在最薄的钙钛矿
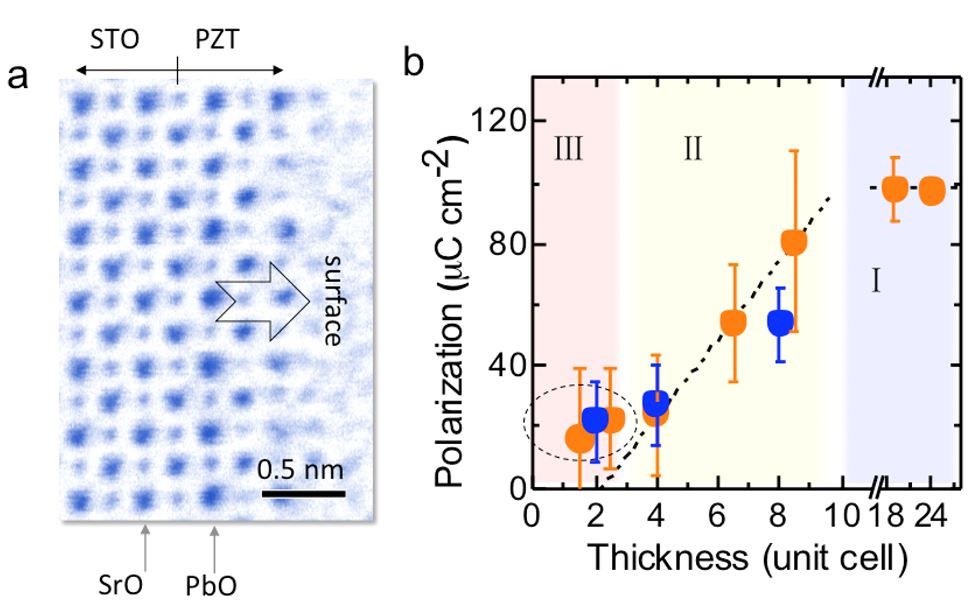
铁电薄膜在数据储存、传感、表面催化等方面...
- 2北京大学-腾讯协同创新实验室关于
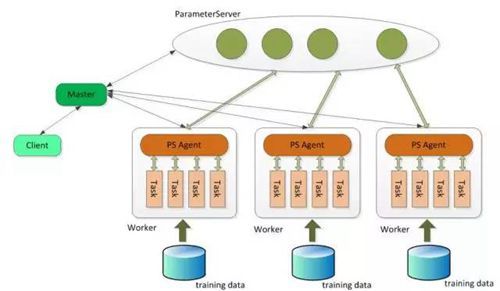
日前,《国家科学评论》(NationalScienceRev...
- 3北京大学乔杰和汤富酬团队合作研

2017年4月27日,北京大学第三医院乔杰教授团...
- 4信息学院杨玉超研究员黄如院士课
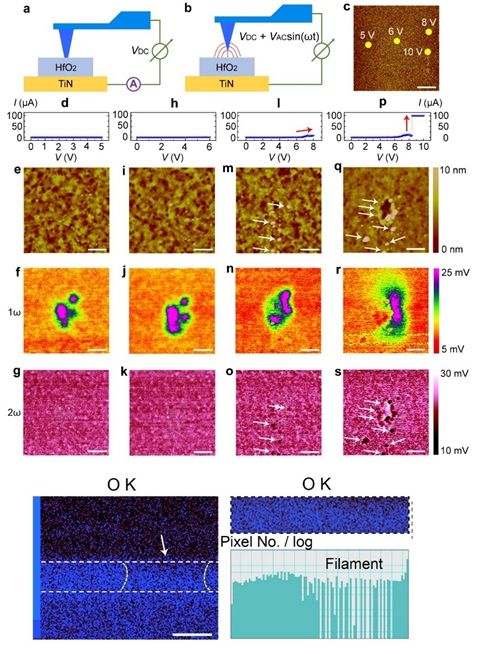
忆阻器是近年来备受关注的新型纳米器件,在新...
- 5工学院陈匡时课题组在单分子成像
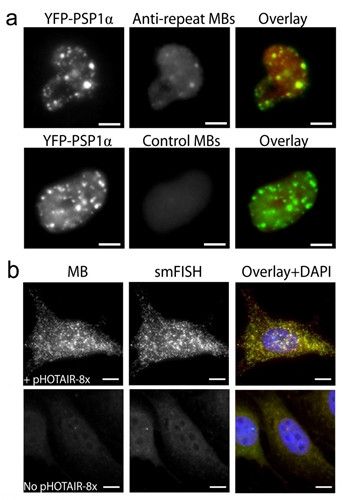
最近,北京大学工学院生物医学工程系陈匡时课...



